

总机:025-58361106-801
传真:025-58361107-806
Email:info@njpeptide.com
地址:南京市化学工业园区方水路158号三楼

“困难序列”对策大全
在固相多肽合成中,“困难序列”现象如同一道无形的墙,当合成进行到特定长度(通常15-20个残基)或富含特定氨基酸模式时,偶联与脱保护效率会突然崩溃。这并非偶然失败,而是由肽链内在的物理化学性质决定的必然挑战。本文将系统性地解构“困难序列”的形成机理——以链间β-折叠聚集为核心,并提供一套从基础优化到“化学手术”的逐级递进的完整解决方案库,重点阐释 伪脯氨酸 与 Hmb 等骨架临时保护基如何作为终极手段,通过重塑肽链性质来攻克这一合成顽疾。
“困难序列”的本质是树脂上生长的肽链发生物理聚集,导致反应位点(N端氨基)被包埋,试剂无法接近。其核心驱动力是分子间氢键,主要形成反平行β-折叠片层。
1. 聚集的分子基础:
氢键供体与受体:肽链骨架上的酰胺氮(-NH-,氢键供体)和羰基氧(-C=O,氢键受体)是形成分子间氢键的基本单元。
疏水作用:侧链疏水的氨基酸(如Val, Ile, Phe, Tyr, Trp)倾向于聚集以避开水环境(DMF/NMP中仍含微量水),进一步驱动并稳定了β-折叠结构。
“临界点”效应:当肽链长度达到一定程度(约15-20个残基),分子间相互作用的总和超过某个阈值,便会发生剧烈的、协同性的聚集,导致反应性断崖式下跌。
2. 高风险序列特征:
富含Val, Ile, Tyr, Phe:强烈的疏水性和β-折叠形成倾向。
重复序列:如 (Val-Ile)ₙ,极易形成规则的β-折叠。
长链疏水片段:连续的疏水残基超过5-6个。
N端为Pro或N-甲基氨基酸:其脱保护本身较慢,若后续序列易聚集,则雪上加霜。
面对困难序列,应采取阶梯式的综合策略。下图概括了从预防到根治的完整决策路径:
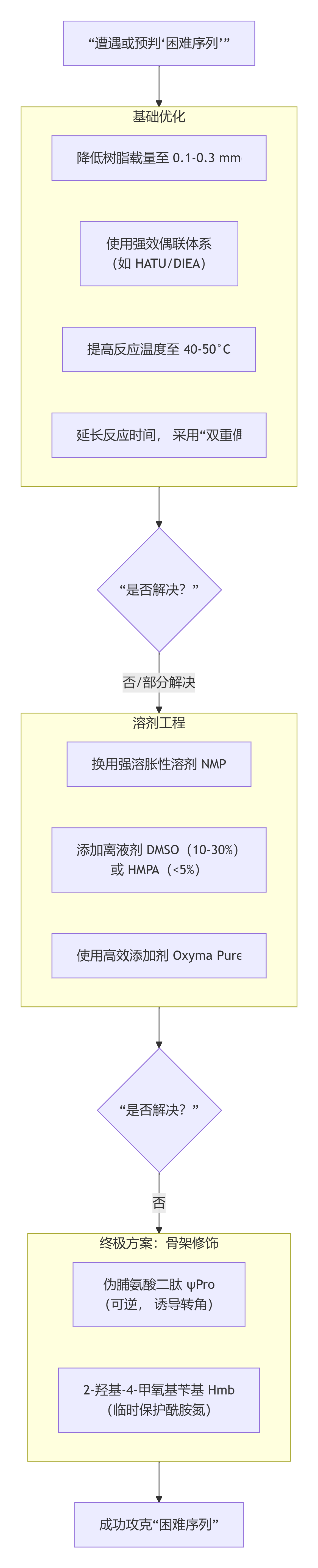
第一级:基础环境优化
这是应对任何潜在困难的第一道防线。
降低树脂载量:将载量从常规的0.4-0.7 mmol/g降至0.1-0.3 mmol/g。这是最有效、最经济的预防措施,直接降低了单位体积内肽链的密度,从根本上减少聚集机会。
使用强效偶联体系:用HATU/DIEA、PyBOP/DIEA等替代DIC/HOBt,其更高的活化效率和形成的活性酯可强行克服因聚集导致的反应惰性。
提高反应温度:将偶联和脱保护温度升至40-50°C。热能破坏氢键,增加肽链和树脂的柔性,改善传质。微波辅助合成是高效实现方式。
延长与多重偶联:对每个残基采用双重甚至三重偶联,确保每一步都尽可能完全。
第二级:溶剂与添加剂工程
若基础优化无效,需改变肽链的溶剂化微环境。
更换主溶剂:NMP对多数树脂的溶胀能力优于DMF,能更好地渗透和溶剂化聚集的肽链。
添加离液剂:DMSO是首选,通常加入10-30%。它是强氢键竞争剂,能有效破坏肽链间的氢键网络。HMPA效果更强,但因毒性已较少使用。
高效添加剂:Oxyma Pure 等不仅能抑制消旋,也有助于改善反应均一性。
第三级(终极方案):骨架临时保护——伪脯氨酸与Hmb策略
当物理方法无法拆解已形成的紧密β-折叠时,必须动用“化学手术”,在合成过程中临时修饰肽链骨架本身,彻底阻断其形成分子间氢键的能力。
1. 伪脯氨酸二肽策略
化学本质:将序列中容易引发聚集的Ser, Thr, Cys(有时也包括Val等)与其C端相邻的氨基酸,以伪脯氨酸二肽的形式引入。
结构:例如,Ser与Xaa形成的伪脯氨酸二肽写作 Fmoc-Ser(ψMe,Mepro)-OH(若Xaa为Met,则类似)。其结构模拟脯氨酸,骨架氮原子参与形成一个五元噁唑烷环,因此该氮原子无法作为氢键供体。
作用机理:
破坏β-折叠:由于缺少氢键供体,伪脯氨酸残基强烈破坏局部β-折叠结构的形成,并诱导β-转角构象。
可逆性:在最终的酸性切割条件下(TFA),噁唑烷环可逆地水解,恢复为原来的两个天然氨基酸(Ser和Xaa)。
应用设计:需在合成前重新规划序列。通常在预测的聚集核心区域,每隔5-6个氨基酸引入一个伪脯氨酸二肽,即可有效阻止长程聚集。这是目前公认的最强效的解决方案。
2. Hmb骨架酰胺保护策略
化学本质:将 2-羟基-4-甲氧基苄基 保护基临时连接到特定氨基酸的骨架酰胺氮上,形成 Fmoc-Hmb-AA-OH 构件。
作用机理:
临时保护:Hmb保护了关键位置的酰胺氢,使其在合成过程中无法形成分子间氢键。
选择性脱除:Hmb对哌啶稳定,但可用非常稀的TFA(如1-2% TFA/DCM)快速、选择性地脱除。脱除后,暴露出游离的酰胺氮和氨基,即可进行下一轮标准的偶联(需先活化脱Hmb后暴露的羧基)。
操作流程:引入Hmb保护的氨基酸后,合成循环变为:脱Fmoc → 洗涤 → 用稀TFA脱Hmb → 洗涤 → 活化并偶联下一个氨基酸 → 洗涤。增加了步骤,但提供了定点、灵活的骨架保护能力。
与伪脯氨酸对比:
伪脯氨酸:更强效,但需要成对替换氨基酸,且设计更复杂。
Hmb:可单独引入任何位置,灵活性极高,但合成循环更繁琐。
目标序列:H-Val-Ile-Val-Ile-Ala-Ile-Val-Ile-Lys-OH
预防性设计:直接采用低载量PAL树脂(0.15 mmol/g)。
溶剂体系:全程使用 NMP 并添加 10% DMSO。
偶联方案:使用 HATU/DIEA(4倍当量),在 45°C 下进行双重偶联,每次60分钟。
终极准备:若上述方法仍失败,则需重新设计,将序列中的 Ile-Ala 替换为 Fmoc-Ile(ψMe,Mepro)-OH(伪脯氨酸二肽)进行合成。
在线监测:观察脱保护时UV曲线是否延迟、基线是否升高,可早期提示聚集。
茚三酮测试:持续阳性是聚集发生的明确信号。
取样分析:在怀疑位点切割少量树脂进行质谱分析,确认缺失序列的位置。
“困难序列”是多肽合成中物理化学规律作用的必然体现,而非随机故障。应对它,需要从被动应对转向主动设计。通过由浅入深的策略组合——从降低载量、优化溶剂,到动用伪脯氨酸或Hmb进行骨架层面的“化学重构”——合成者能够系统性地化解聚集这一核心矛盾。掌握这套对策大全,特别是理解伪脯氨酸和Hmb通过消除氢键供体来根除聚集的化学本质,意味着获得了合成任意长链、任意序列多肽的终极信心与能力。这标志着多肽合成技术从处理“友好”序列,迈向征服所有“敌对”序列的成熟阶段。
南京肽业YM说多肽|“困难序列”对策大全:从聚集机理到伪脯氨酸、Hmb骨架修饰的终极方案