

总机:025-58361106-801
传真:025-58361107-806
Email:info@njpeptide.com
地址:南京市化学工业园区方水路158号三楼

侧链保护基设计原理(酸性篇):
Asp/Glu的保护策略与酯化副反应防控
在天冬氨酸与谷氨酸的保护化学中,侧链羧基的酯化保护远非一个简单的“屏蔽”操作。它是一场与分子内反应动力学的精密博弈。本文旨在深入剖析Asp/Glu保护的核心矛盾:如何在有效防止侧链干扰主链偶联的同时,规避由酯基自身引发的、特别是天冬氨酸的环化副反应。我们将系统梳理从经典OtBu到高级OAllyl、O-2-苯基异丙酯等一系列保护基的化学逻辑,并提供一套基于序列分析的理性选择策略。
Asp与Glu的侧链羧基若在合成中保持游离,将带来两个主要问题:
竞争性活化与分支:在活化α-羧基进行偶联时,侧链羧基同样可能被活化,导致产生分支肽或导致同一分子内发生环化,严重降低目标线性产物的产率。
质子源与消旋:游离羧基可作为质子源,在某些偶联机制中加剧α-碳的消旋化。
因此,将其转化为化学惰性的酯(通常是叔丁酯,OtBu)是Fmoc-SPPS的标准操作。
OtBu的优势:
出色的稳定性:对Fmoc脱除条件(哌啶)绝对稳定,仅在最终强酸切割(如TFA)时脱除,符合Fmoc策略的正交性要求。
适中的空间位阻与成本:相对于更复杂的保护基,其合成简单,价格低廉,是绝大多数序列的首选。
OtBu的“阿喀琉斯之踵”——天冬酰胺的形成:
当天冬氨酸(Asp)的C端连接的是甘氨酸、丝氨酸、丙氨酸等空间位阻小、氮原子亲核性强的氨基酸时,其侧链OtBu酯在偶联试剂(特别是碳二亚胺类如DIC)或碱的存在下,可能发生分子内亲核进攻,形成一个高反应活性的五元环琥珀酰亚胺中间体。
此中间体随后可被水或亲核试剂进攻并开环,产生两种主要副产物:
α-肽键异构体:正常的α-羧基连接。
β-肽键异构体:侧链β-羧基参与形成主链肽键,导致主链连接点从α-碳转移到β-碳,此过程称为异构化。β-天冬氨酸残基在自然界和生物制药中是一种重要的、通常非预期的修饰,会改变多肽的结构与功能。
为防止环化,化学家发展出了几种策略,核心思路是增加空间位阻或改变脱除机制。
增大空间位阻:OtPe与O-2-PhiPr
OtPe:叔戊酯。在OtBu的叔丁基上增加一个甲基,空间位阻显著增大,能有效阻碍分子内环化的过渡态形成。其酸敏感性与OtBu类似,在标准TFA切割中脱除。是解决Asp后接小位基氨基酸序列的首选升级方案。
O-2-PhiPr:2-苯基异丙酯。其空间位阻极大,且拥有超酸敏感性。它能在极低浓度的TFA(如0.5%)或稀盐酸中快速、优先脱除,而其他tBu等保护基保持稳定。
高级应用:用于合成后修饰或环化。例如,在合成含Asp的环肽时,可在完成线性链组装后,用弱酸选择性脱去Asp侧链的O-2-PhiPr保护,暴露出羧基以进行分子内环化,而其他氨基酸的侧链保护完好。这避免了在最终强酸切割时进行高稀释度的环化,效率更高。
正交保护策略:OAllyl及其脱除
OAllyl:烯丙酯。其脱除机制与酸、碱均不同,需在钯催化剂存在下进行。
脱除条件:在固相或溶液中,使用Pd(PPh₃)₄和亲核试剂(如苯硅烷、N-甲基苯胺)进行催化转移,可温和、选择性地将OAllyl脱除,生成游离羧基和丙烯。
核心优势:与Fmoc/tBu体系完美正交。在合成中途,可选择性脱除Asp/Glu的OAllyl保护以进行环化或修饰,而其他所有保护基(包括Fmoc)均不受影响。是合成复杂环肽或修饰肽的强力工具。
注意事项:钯催化剂可能价格昂贵,且需注意其对含硫氨基酸(如Cys, Met)的潜在影响。
面对一个含有Asp/Glu的序列,可按以下逻辑选择保护基:
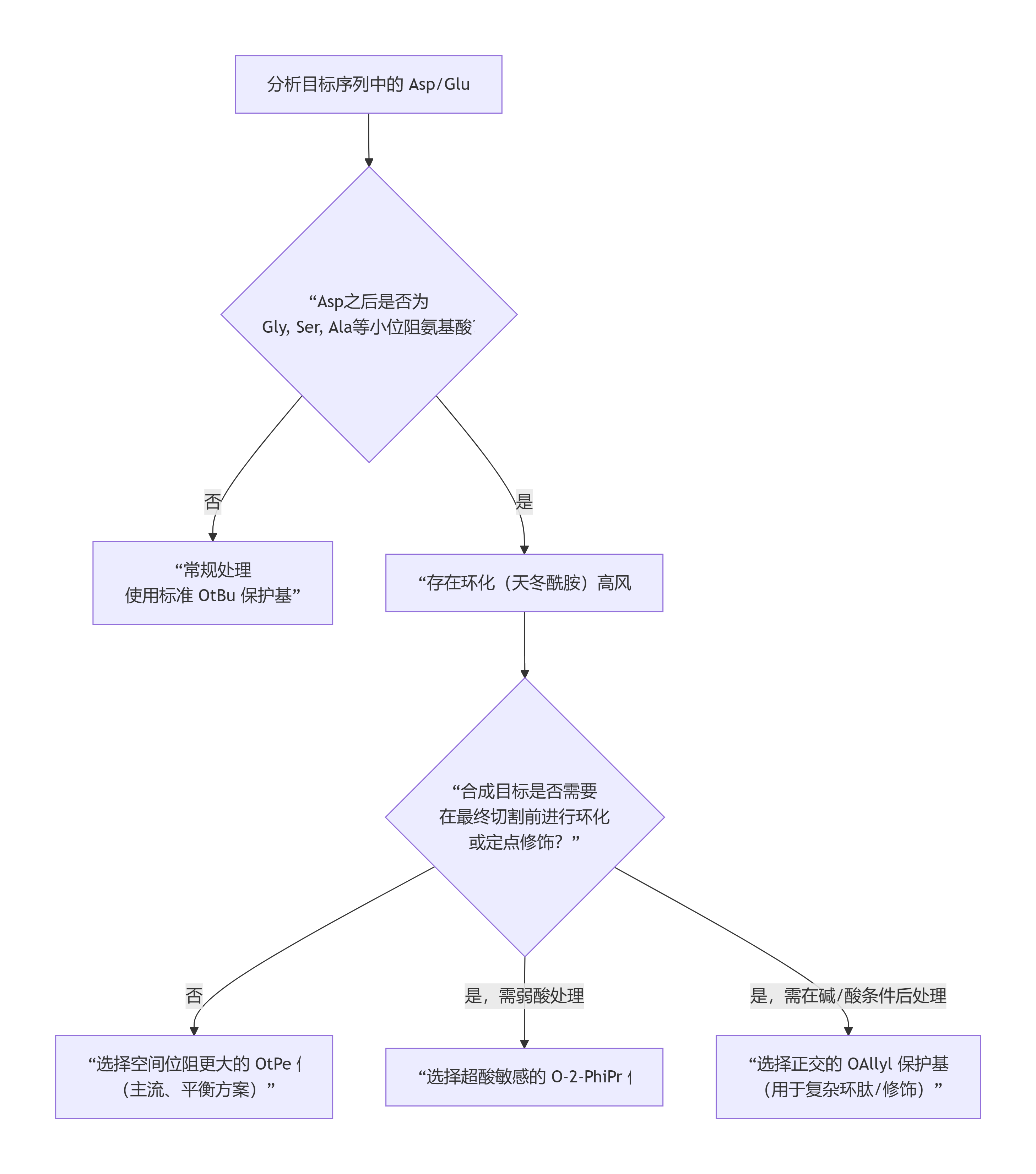
五、谷氨酸的特殊性
谷氨酸的环化倾向远低于天冬氨酸,因其形成的是热力学不利的六元环。因此,Glu在绝大多数情况下使用标准的OtBu保护即可,仅在极其特殊的序列(或与Glu类似的结构要求)中才需考虑上述进阶策略。
无论选择何种保护基,在合成长肽或敏感序列时,建议:
分析粗肽:使用HPLC-MS仔细检查粗产物,寻找比目标肽保留时间稍早或稍晚的、分子量相同的杂质峰,这常是α/β异构体的特征。
诊断性合成:对于全新的高风险序列(如Asp-Gly-Asp),可先合成一个包含该模体的短肽(如五肽),快速评估环化程度,再决定长肽合成的保护策略。
对Asp/Glu的保护,是多肽合成中“细节决定成败”的典范。从默认的OtBu到防控环化的OtPe,再到为复杂结构设计服务的O-2-PhiPr和OAllyl,这一系列保护基的演进,体现了从解决基础问题到实现高阶合成设计的化学智慧。掌握这些工具及其背后的机理,意味着您不仅能避免一个常见的合成陷阱,更能主动设计合成路线,以精准可控的方式,构建那些含有敏感位点却功能重要的多肽结构。
南京肽业YM说多肽|侧链保护基设计原理(酸性篇):Asp/Glu的保护策略与酯化副反应防控